影响电极电势的因素及电极电势的应用
上一节
下一节
1. 影响电极电势的因素:
内因 ----电极的热力学过程
外因----浓度、 pH 、沉淀 、 配合物 、温度
2. Nernst 公式
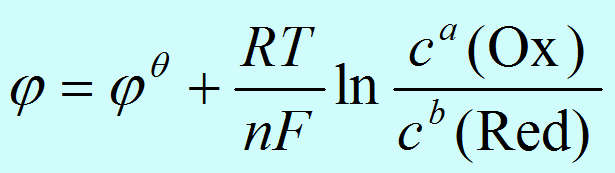
增大电对中氧化型的浓度,电极电势增大。也说明电对中氧化型的氧化能力增强或还原型的还原能力减弱,反之亦然。
大多数含氧酸盐的氧化能力随酸度增大而增强。
在电对溶液中加入沉淀剂,若使氧化态物质生成沉淀,则电极电势降低,氧化态物质的氧化能力减弱,稳定性增加。沉淀物Ksp越小,电极电势越低。若还原态物质生成沉淀,则电极电势升高,结果正好相反。
在电对Mn+/M 溶液中加入配位剂,若使Mn+生成配离子,则电极电势降低, Mn+的氧化能力减弱, M 还原性增强。配离子Kf 越大,电极电势越低。


